2022师大附中中考化学模拟试题
第一卷(选择题60分)
本卷共16道分题,每道分题3分,共48分。每题给出的四个选项中,只有一个是最合适的。
1.碳酸钠和碳酸氢钠是两种常见的金属钠碳酸盐,广泛应用于生产和生活中。下列关于碳酸钠和碳酸氢钠的说法不正确的是()
A.nahco3能中和胃酸,对胃壁无强烈刺激和腐蚀,可用于治疗胃酸过多,但不适用于胃溃疡患者。
B.nahco3可以中和面粉发酵产生的酸,产生二氧化碳气体,可以用来做馒头。
C.当NaHCO3混合在C.Na2CO3溶液中时,不能通过加热溶液将其除去。
d .向Na2CO3的饱和溶液中通入CO2气体,得到NaHCO3沉淀,表明Na2CO3的溶解度高于NaHCO3。
2.设NA为avo伽德罗常数的数值,下列说法正确的是()。
0.2molH2O2完全分解转移的电子数为0.4NA
在25和101kPa下,16gO3和O2混合气体中的氧原子数为NA。
将0.1摩尔三氯化铁饱和溶液滴入沸水中形成的胶体粒子数为0.1纳
1摩尔弗溶于过量稀硝酸,电子转移数为3NA。
在标准条件下,22.4LCHCl3中所含的氯原子数为3NA。
A.B.C.D.
3.下列关于NA的说法正确的是()
A.如果一个无水乙醇与足够的金属钠反应生成5.6LH2(标准温度和压力),乙醇分子中的共价键总数为4NA。
B.在标准温度和压力下,22.4L甲烷和22.4L氯气在光照下充分反应,生成的CH3Cl分子数必须为NA。
c .向密闭容器中加入1.5摩尔H2和0.5摩尔N2,充分反应,得到分子数为NA的NH3
d .在常温常压下,将56g铁片放入足量的浓硫酸中,生成分子数为NA的SO2
4.下列叙述或实验现象描述正确的是()
A.铜与浓硫酸共热产生气体使石蕊溶液变红,表明浓硫酸是酸性的。
b .在足量铁与稀硝酸反应后,向溶液中滴加KSCN溶液,溶液变为血红色。
C.向FeSO4溶液中通入NO2气体,溶液中无明显现象。
d、向BaCl2溶液中通入SO2气体,然后通入NH3,生成白色沉淀。
5.下列说法正确的是()
A.在一种溶液中加入稀NaOH溶液,不会产生刺激性气体,说明溶液中一定不含NH4。
B.NaCl固体中混合的NH4Cl可以通过加热去除,说明NH4Cl会升华。
C.C.SO2气体和Cl2都能使品红溶液褪色,说明二者都有较强的氧化性。
D.浓硫酸可以用来干燥H2、Cl2、SO2等气体,说明浓硫酸具有吸水性。
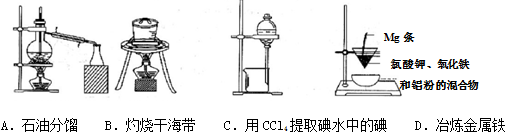
6.下列实验装置或操作不符合实验要求的是()
7.已知有2fe32i ~ 2fe2i2、Br2 2Fe2、2Br 2Fe3。现在,将一定量的氯气引入含有FeBr2和FeI2的溶液中,然后在反应后将少量KSCN溶液滴入溶液中。结果,溶液变成红色,这在下面的描述中是正确的
按I、Fe2、Br的顺序,还原性逐渐减弱;
原液中的br必须被氧化;
通入氯气后,原液中的Fe2必须被氧化;
不确定通入氯气后溶液中是否还存在Fe2
如果取少量所得溶液,加入CCl4,充分摇匀,然后静置,再向上层溶液中加入足够的AgNO3溶液,只会产生白色沉淀,说明原液中的Fe2和Br被完全氧化。
A.B.C.D.
8.保护环境已经成为人类的共识。以下做法不利于环境保护
A.来自火电厂的煤被粉碎和脱硫。
B.电镀废液经中和后直接排入农田。
C.聚乳酸塑料替代传统塑料作为购物袋
D.PVC塑料废弃物的回收与合理处理
9.关于营养素的说法是对的。
A.淀粉和稀硫酸一起加热后,向溶液中滴加银氨溶液,检查葡萄糖
10.下列关于金属冶炼的说法是正确的。
a .工业上可以通过铝热反应冶炼大量金属铁
B.金属钠、铝和铜可用热还原法制备。
当C. Co还原磁铁矿得到9mol铁时,转移24mol电子。
d .电解饱和氯化镁溶液,得到金属镁。
1.2015年11月29日至30日,***主席出席气候变化巴黎大会,各国在会上探讨如何应对气候变化,提高经济绿色化水平,实现人类可持续发展。实现“一口气”
,共奋斗”全国各地为治理雾霾广泛开展了一系列活动。下列活动不符合这一主题的是()A.机动车实行限行措施是减少雾霾的途径之一
B.积极推广风能、太阳能、氢能等新型能源的使用
C.将秸秆焚烧可得富含钾肥的草木灰,焚烧是一种较为理想的秸秆处理办法
D.通过吸收空气中CO2并利用廉价能源合成汽油可推广“绿色自由”计划
12.下列文字表述与反应方程式对应且正确的是()

13.化学与生活密切相关。下列说法正确的是()
A.福尔马林可作食品的保鲜剂
B.乙烯可作水果的催熟剂
C.做衣服的棉和麻均与淀粉互为同分异构体
D.磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
14.自然环境与人们的生活息息相关。下列有关环境问题的说法不正确的是()
A.氟利昂(CCl2F2)因破坏大气臭氧层而导致“温室效应”
B.将垃圾分类并回收利用是垃圾处理的发展方向
C.废旧电池的回收,其主要目的是保护环境,而不是回收金属
D.淀粉餐具被认为是有发展前景的一次性餐具,可有利于保护环境
15.化学与环境、材料、信息、能源关系密切,下列说法正确的是()
A.绿色化学的核心是应用化学原理对环境污染进行治理
B.开发高效氢能、太阳能等新型电动汽车,以解决城市机动车尾气排放问题
C.PM2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体
D.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅
16.化学与人类生产、生活密切相关,下列说法正确的是
A.蚕丝和棉花的组成元素相同,结构不同,因而性质不同
B.汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的
C.古代的陶瓷、砖瓦、现代的玻璃、水泥等,都是硅酸盐产品
D.工业上通过电解熔融的氯化物制取Na、Mg、Al三种金属
第Ⅱ卷非选择题(共6小题,52分)
17.M是一种新型可生物降解的高分子材料,主要制造可降解纤维、塑料和医用材料,其水解最
终产物为N。燃烧9.0g的N只产生CO2和H2O,且质量分别为13.2g和5.4g,实验测得N在标准状况下的蒸气密度为4.02g/L;N的核磁共振氢谱显示的峰面积之比为1:1:1:3。
(1)通过计算确定N的分子式
(2)写出N的结构简式,并写出N在催化剂条件下缩聚反应合成M的化学方程式.
18.国家规定,酿造食醋的总酸含量标准为3.5~5.0g/100mL(总酸含量即100mL食醋中CH3COOH的质量).某化学兴趣小组为测定某市售食醋的总酸含量,进行了实验.实验后,得知10.0mL该食醋样品与7.5g溶质的质量分数为4%的氢氧化钠溶液恰好完全反应.计算该市售食醋样品中的总酸含量,并说明是否符合国家标准.(假设该市售食醋样品中其他物质不与氢氧化钠发生反应)
19.叶绿素在光的作用下可将CO2和H2O转化为葡萄糖(C6H12O6)和O2,

叶绿素有a、b两种,已知某种叶绿素中仅含有C、H、O、N、Mg五种元素,且知该叶绿素中各元素的质量分数分别是:
w(C)=73.99%w(H)=8.072%w(O)=8.969%w(N)=6.278%w(Mg)=2.691%
经测定该叶绿素的相对分子质量小于1000,试确定该叶绿素的分子式。
20.近期,我国个别企业违法排污导致地下
水严重污染又成为媒体焦点。对水的质量监控
有很多指标,其中水中溶解氧(DO)的多少是衡量水体自净能力的一个指标。
I.对溶解氧(DO)的测定步骤是:
①在一定温度下量取100.00mL新鲜水样,在碱性条件下使其中的O2将Mn2+氧化为MnO(OH)2:
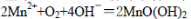
②向步骤①反应后的溶液中加入KI溶液,使其中生成的MnO(OH)2再还原成Mn2+:
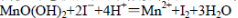
③最后用0.0100mol·L-1Na2S2O3标准溶液滴定步骤②中生成的I2:
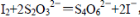
消耗Na2S2O3标准溶液11.00mL。
(1)步骤③使用的指示剂是淀粉试液。滴定终点时指示剂的颜色变化情况是____。
(2)硫代硫酸(H2S2O3)是一种二元弱酸。步骤③应选用____滴定管进行滴定,结合离子方程式说明原因:______。
(3)水样中溶解氧(DO)的浓度为mg·L-1。
II.该实验需用Na2S2O3固体配制100mL0.0100mol·L-1Na2S2O3标准溶液。
(4)请按配制的过程填写选用仪器的顺序:____(填编号)。
①玻璃棒②胶头滴管③100mL容量瓶④天平⑤25mL烧杯
(5)配制0.0100mol·L-1Na2S2O3标准溶液时,下列操作使所配溶液浓度偏高的是____。
A.没有用蒸馏水洗涤烧杯
B.定容时俯视容量瓶刻度线
C.配制前容量瓶洗净后没干燥
D.摇匀后见液面下降,再加水至刻度线
E.用天平称量药品时,左盘低,右盘高
21.(6分)下表是某“加碘食盐”包装袋上的部分文字说明。
经测定,该“加碘食盐”中KIO3的含量为42.8mg·kg-1。计箅每千克“加碘食盐”中KIO3的物质的量为 mol,该“加碘食盐”的含碘量为 mg·kg-1。
(2)将5.0g该“加碘食盐”溶于水中配成100mL溶液,该溶液中IO离子物质的量浓度为mol·L-1。
22.(12分)为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下
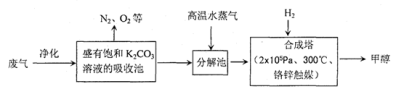
(1)合成塔中反应的化学方程式为;△H<0。从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了。
(2)从合成塔分离出甲醇的原理与下列操作的原理比较相符(填字母)
A.过滤B.分液 C.蒸馏D.结晶
工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施。“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括.
(3)在体积为2L的合成塔中,充人2molCO2和6molH2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
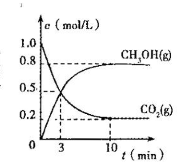
从反应开始到平衡,V(H2)=_____;能使平衡体系中nCH3OH)/n(CO2)增大的措施有_____。
(4)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
巳知
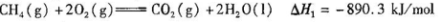

写出C02(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式____。
好消息:广东地区未达到普高分数线的同学,可点击下方按钮咨询客服,就有机会报读高职高考班,获取职校报考全日制大专、本科名额!
 中学
中学
 大学
大学
